重庆市南开中学2016届二模理科综合试题及答案(4)

34.【物理一选修3-4】(15分)
(1)(5分)一振动周期为T,振幅为A,位于x=0点的波源从平衡位置沿y轴正向开始做简
谐振动,该波源产生的一维简谐横波沿x轴正向传播,波速为v,传播过程中无能量损失,一
段时间后,该振动传播至某质点P,关于质点P振动的说法正确的是 。
A.振幅一定为A
B.周期一定为T
C.速度的最大值一定为v
D.开始振动的方向沿y轴向上或向下取决于它离波源的距离
 E.若P点与波源距离s=vt,则质点P的位移与波源的相同
E.若P点与波源距离s=vt,则质点P的位移与波源的相同
(2)(10分)一半圆柱形透明物体横截面如图所示,底面AOB镀银(图中粗线),O表示半圆截面的圆心。一束光线在横截面内从M点的入射角为30℃,∠MOA=60°,∠NOB=30°。求:
(i)光线在M点的折射角; (ii)透明物体的折射率.
35.【物理—选修3-5】(15分)
 (1)(5分)下列说法正确的是:
(1)(5分)下列说法正确的是:
A.在康普顿效应中,当入射光子与晶体中的电子碰撞时,把一部分动量转移给电子,因此,光子散射后波长变长
B.考古学家发现某一骸骨中碳14的含量为活着的生物含量的四分之一,已知碳14的半衰期为5730年,则确定该生物死亡距今11460年
C.按照波尔理论,氢原子核外电子从较小半径跃迁到较大半径轨道时,电子的动能减少,原子总能量增大
D.卢瑟福发现了中子,汤姆孙发现了电子
E.机场、车站等地方进行安检工作时,能轻而易举地窥见箱内物品,利用了γ射线较强的穿透能力
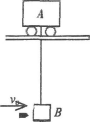
(2)(10分)如图所示,光滑悬空轨道上静止一质量为2m的小车A,用一段不可伸长的轻质细绳悬挂一质量为m的木块B.一质量为m的子弹以水平速度v0射人木块B并留在其中(子弹射入木块时间极短),在以后的运动过程中,摆线离开竖直方向的最大角度小于90°,试求:
(i)子弹射入木块时损失的机械能; (ii)木块能摆起的最大高度.
36.【化学——选修2:化学与技术】(15分)
 工业生产玻璃会产生大量的窑炉气(含SO2和氮氧化物等)。为减少环境污染,某工厂生产玻璃与处理窑炉气的工艺流程如图:
工业生产玻璃会产生大量的窑炉气(含SO2和氮氧化物等)。为减少环境污染,某工厂生产玻璃与处理窑炉气的工艺流程如图:
(1)生产普通硅酸盐玻璃的主要原料是石英砂、______和石灰石。其中,石灰石参与的反应方程式是_______________。
(2)窑炉气中的SO2一部分来源于原料中添加剂Na2SO4的热分解,该反应方程式为___________;
氮氧化物主要源于空气中N2与O2的反应,该类气体在高温下基本无色,随温度的降低逐渐变为红棕色,原因是________________________________________________。
(3)“脱硫塔”中反应形成的灰分,除亚硫酸钠和氮的含氧酸盐外,主要还有__________;用于喷雾的火碱溶液应选用软化水配制,原因是____________________________________________________。
(4)在“脱硝装置”中,催化剂设计成蜂窝而非平板状结构,原因是____________________________。
氨水在脱硝过程中的作用是____________________________________________________________。
(5)净化气的主要成分是________________________________________________________________。
37.【化学——选修3:物质结构与性质】(15分)
自然界存在的元素中,金属元素种类更多,非金属元素丰度更大。
I.80%左右的非金属元素在现代技术包括能源、功能材料等领域占有极为重要的地位。
(1)氮及其化合物与人类生产、生活息息相关,基态N原子中电子在2p轨道上的排布遵循的原则是________,N2F2分子中N原子的杂化方式是____________,1 mol N2F2含有______个σ键。
(2)高温陶瓷材料Si3N4晶体中键角N—Si—N________Si—N—Si(填“>”“<”或“=”),原因是_________。
II.金属元素在现代工业中也占据极其重要的地位,如以古希腊神话中“泰坦”(Titan)的名字命名的钛(Titanium)元素,意指“地球的儿子”,象征此物力大无穷。钛也被称为“未来的钢铁”,具有质轻,抗腐蚀,硬度大,是宇航、航海、化工设备等的理想材料,是一种重要的战略资源,越来越受到各国的重视。
(1)基态钛原子核外共有________种运动状态不相同的电子。金属钛晶胞如下图1所示,为_______堆积(填堆积方式)。
(2)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图2。化合物乙的沸点明显高于化合物甲,主要原因是________________。化合物乙中采取sp3杂化的原子的电负性由大到小的顺序为__________。


(3)钙钛矿晶体的结构如右图所示。假设把氧离子看做硬球接触模型,钙离子和钛离子填充氧离子的空隙,氧离子形成正八面体,钛离子位于正八面体中心,则一个钛离子被__________个氧离子包围;钙离子位于立方晶胞的体心,一个钙离子被_____个氧离子包围。钙钛矿晶体的化学式为__________。若氧离子半径为a pm,则钙钛矿晶体中两个钛离子间最短距离为_______pm,钛离子与钙离子间最短距离为_______pm。
38.【化学——选修5:有机化学基础】(15分)
 中国科学家屠呦呦因青蒿素的研究荣获了2015年诺贝尔化学奖。青蒿素是继乙氨嘧啶、氯喹、伯喹之后最有效的抗疟特效药,具有速效和低毒的特点,曾被世界卫生组织称做是“世界上唯一有效的疟疾治疗药物”。由青蒿素合成系列衍生物(它们的名称和代号如图所示)的路线如图:
中国科学家屠呦呦因青蒿素的研究荣获了2015年诺贝尔化学奖。青蒿素是继乙氨嘧啶、氯喹、伯喹之后最有效的抗疟特效药,具有速效和低毒的特点,曾被世界卫生组织称做是“世界上唯一有效的疟疾治疗药物”。由青蒿素合成系列衍生物(它们的名称和代号如图所示)的路线如图:
回答下列问题:
(1)青蒿素的分子式为________;氢化青蒿素分子中官能团名称为______________。
(2)反应①中,有机反应类型为___________;NaBH4的作用是_______________。
A.氧化剂 B.还原剂 C催化剂 D、溶剂
(3)有机物D是分子式为C4H4O3的五元环状化合物,请写出反应③的化学反应方程式_________。
(4)青蒿唬酯能够发生的反应类型有________。
A.酯化反应 B.水解反应 C.还原反应 D.加聚反应
(5)以H2Q表示双氢青蒿素,写出反应②的化学方程式__________________________。
(6)从双氢青蒿素(H2Q)出发,可通过多步反应合成出有机物E。合成过程中,有机原料除H2Q、 外,还需含苯环的二羟基化合物F,写如有机物F与NaOH溶液反应的离子反应方程式___________________________,有机物G是F的同分异构体,有机物G遇FeCl3溶液显紫色,且有4种不同类型的氢,其个数比为3:2:2:1,则符合条件的有机物G的同分异构体有_____种。
外,还需含苯环的二羟基化合物F,写如有机物F与NaOH溶液反应的离子反应方程式___________________________,有机物G是F的同分异构体,有机物G遇FeCl3溶液显紫色,且有4种不同类型的氢,其个数比为3:2:2:1,则符合条件的有机物G的同分异构体有_____种。
39.【生物——选修1:生物技术实践】(15分)
40.【生物——选修3:现代生物技术专题】(15分)
下图是利用现代生物工程技术治疗遗传性糖尿病的过程图解。请据图回答下列问题:
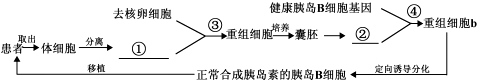
(1)图中②所示的生物技术的供体细胞一般都选用传代10代以内的细胞,这是因为________;图中③所示的细胞名称是______________。
(2)重组细胞A培养过程所用的培养液与植物组织的培养基从成分上主要区别是前者必须含有___________。重组细胞A培养过程中所需要的基本条件包括充足的营养、_______、______、气体环境。
(3)④所示的生物技术名称是____________,若想得到大量健康的胰岛B细胞的胰岛素基因,可利用_______技术。
- 上一篇:2016山东青岛理综一模试题及答案
- 下一篇:2016年高考理综模拟试题